Analfistel, Verschluss mit Anal Fistula Plug® (AFP®) - Allgemein- und Viszeralchirurgie
Sie haben keine Lizenz erworben - paywall ist aktiv: zur Produktauswahl
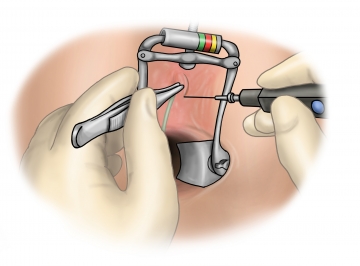
Exzision des Fistelostiums
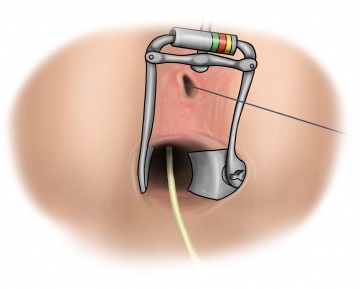
Einziehen des Plugs
Fixierung des Plugs
Aktualisierung vom: 01.10.2022
Publikation vom: 17.05.2021
Einzelfreischaltung
Freischaltung auf diesen Lehrbeitrag
für 3 Tage
4,99 € inkl. MwSt.

webop-Account Single
Freischaltung aller Lehrbeiträge
Preis pro Monat
für das Modul: Allgemein- und Viszeralchirurgie