Nabelhernienreparation, offen, präperitoneale umbilikale Mesh-Plastik („PUMP“-Repair) - Allgemein- und Viszeralchirurgie
Sie haben keine Lizenz erworben - paywall ist aktiv: zur Produktauswahl
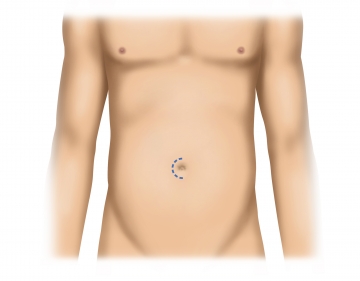
Hautschnitt
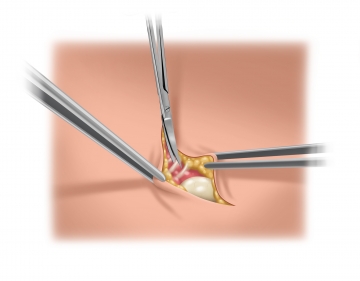
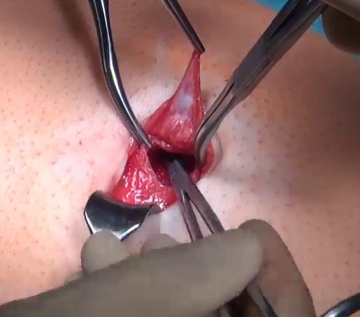
Präparation des Bruchsacks
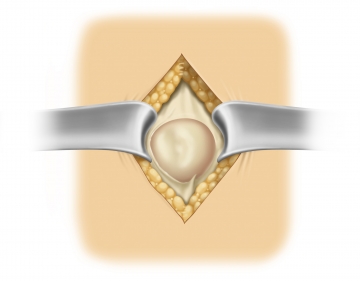
Zirkuläres Darstellen der Faszienränder
Präparation des präperitonealen Raums
Vorbereiten des Meshs
Platzieren des Meshs
Verschluss der Faszienlücke
Refixierung des Nabels; Wundverschluss
Aktualisierung vom: 10.04.2024
Publikation vom: 29.04.2013
Einzelfreischaltung
Freischaltung auf diesen Lehrbeitrag
für 3 Tage
4,99 € inkl. MwSt.

webop-Account Single
Freischaltung aller Lehrbeiträge
Preis pro Monat
für das Modul: Allgemein- und Viszeralchirurgie