Narbenhernienoperation, laparaskopisch mit Ventralight™ ST Netz und ECHO PS™ Positionierungs- System - Allgemein- und Viszeralchirurgie
Sie haben keine Lizenz erworben - paywall ist aktiv: zur Produktauswahl
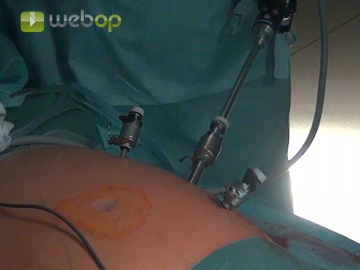
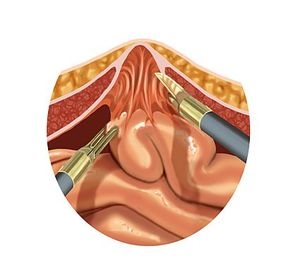
Trokarpositionierung
Das Pneumoperitoneums wird durch eine links subkostal platzierte Veress-Kanüle angelegt. Im Höhe der vorderen Axillarlinie wird im Mittelbauch stumpf der Kanal für den ersten Trokar geschaffen. Unter diaphanoskopischer und laparoskopischer Kontrolle werden jeweils 5 cm kranial und kaudal ein 5mm-Trokar zusätzlich eingebracht.
Bemerkung: Der zunächst platzierte 10mm-Trokar wird später zur Netzplatzierung gegen einen 12mm-Trokar ausgetauscht.
Adhäsiolyse mit Darstellung der Bruchpforte
Die explorative Laparoskopie zeigt eine große Hernie sowie ausgedehnte Adhäsionen im Bereich derselben. Es erfolgt nun mit der Schere Schritt für Schritt die Adhäsiolyse der zur Bauchdecke hochgezogenen Dünndarmschlingen und des großen Netzes. Die Bruchpforte kann so gut dargestellt werden.
Tipp: Die Lösung der Verwachsungen wird ausschließlich mit der Schere ohne Strom oder Ultraschall vorgenommen. Nur so lassen sich thermische Schäden mit sekundärer Darmperforation vermeiden. Bei ausschließlich scharfer Dissektion dringt Kohlendioxid in die Adhäsionen ein und vergrößert so die Distanz zwischen adhärenten Strukturen und Bauchwand.
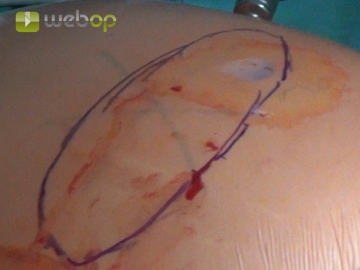
Ausmessen der Netzgröße
Mit einer jeweils perkutan eingestochenen Kanüle werden die Ränder der Bruchlücke markiert und auf die vordere Bauchwand angezeichnet. Man wählt ein 17 × 23 cm großes Ventralight-Netz mit integriertem Positionierungssystem der Firma Bard, um die Bruchlücke in alle Richtungen ausreichend weit, mindestens 5 cm, zu bedecken.
Bemerkung: Die besondere Beschichtung des Ventralight-Netzes mit Hyaluronsäure-Carboxymethylzellulose hat zuletzt die beste klinische Wirksamkeit zur Adhäsionsprophylaxe nachgewiesen(Evidenzlevel Ib).
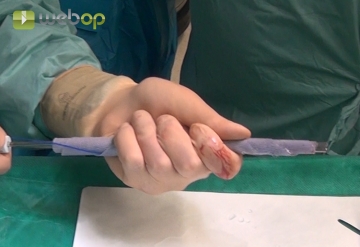
Einbringen des Netzes
Zunächst wird die obere Inzision für die Kamera auf einen 10mm-Trokar erweitert, anschließend der mittlere 10mm-Trokar gegen einen 12mm-Trokar ausgewechselt. Das Netz wird befeuchtet und auf der Einführungshilfe möglichst eng aufgerollt. Anschließend wird es durch einen 12mm-Trokar in die Bauchhöhle eingebracht.
Bemerkung: Alternativ kann der Trokar auch entfernt und das Netz durch dessen Kanal nach intraabdominell eingeführt werden.
Positionierung des Netzes
Fixation des Netzes
Entfernung des Haltesystems; Double-crown-Technik
Verschluss der Inzisionen
Einzelfreischaltung
Freischaltung auf diesen Lehrbeitrag
für 3 Tage
4,99 € inkl. MwSt.

webop-Account Single
Freischaltung aller Lehrbeiträge
Preis pro Monat
für das Modul: Allgemein- und Viszeralchirurgie