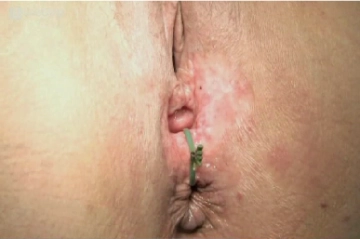
Zunächst Inspektion der mit einer Fadendrainage versorgten reizlos verheilten Fistel. Sondierung der Fistel durch die äußere Fistelöffnug, sowie die digital-rektale Untersuchung.
-
Sondierung und Inspektion der Fistel
![Sondierung und Inspektion der Fistel]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann. -
Exzision des äußeren Fistelostiums
![Exzision des äußeren Fistelostiums]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann.Nun beginnt die trichterförmige Exzision der Fistel entlang des Fistelgangs.
-
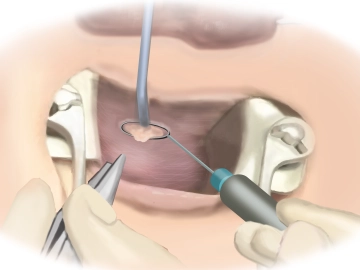
Exzision des inneren Fistelostiums
![Exzision des inneren Fistelostiums]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann.Der Analsperrer wird eingesetzt und die innere Fistelöffnung präpariert. Entlang der Fistel wird nun die innere Fistelöffnung sparsam exzidiert.
Präparation des Verschiebelappens (Advancement Flap)
Der für die Defektdeckung nötige Mukosalappen wird vorsichtig mit dem Elektrokauter präpariert. ...
Der für die Defektdeckung nötige Mukosalappen wird vorsichtig mit dem Elektrokauter präpariert. ...
Jetzt freischalten und direkt weiter lernen.
Einzelfreischaltung
Freischaltung dieses Lehrbeitrags für 3 Tage.
9,40 $
inkl. MwSt.
Beliebtestes Angebot
webop - Sparflex
Kombiniere flexibel unsere Lernmodule und spare bis zu 50%.
ab 7,27 $ / Modul
87,34 $/ jährliche Abrechnung
Allgemein- und Viszeralchirurgie
Alle Lehrbeiträge in diesem Modul freischalten.
14,55 $
/ Monat
174,70 $ / jährliche Abrechnung