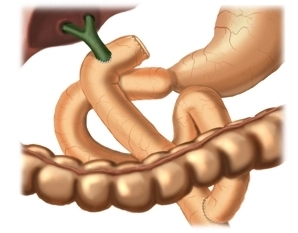
Die Hepatico-Jejunostomie End-zu-Seit mit einer retrokolisch geführten durch Roux-Y-Anastomose aus der Passage ausgeschalteten oberen Jejunumschlinge stellt den Goldstandard der biliodigestiven Anastomose dar.
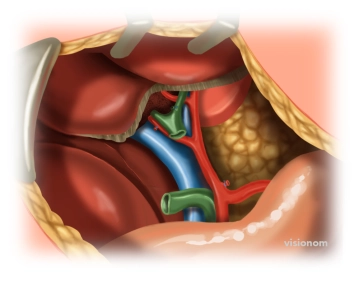
Hierbei wird die biliodigestive Anastomose vorzugsweise oberhalb des Zystikusabgangs und ca. 2–3 cm unterhalb der Hepatikusgabel angelegt.
- Es sollte eine möglichst weite Anastomosenöffnung geschaffen werden (ist der Gallengang zu eng , empfehlen sich Erweiterungsplastiken z.B. nach Hepp-Couinaud).
- Die Naht mit einreihig allschichtigen Einzelknopfnahtreihen sollte primär dicht sein.
- eine exakte Adaptation von Galle- und Darmschleimhaut muss angestrebt werden.