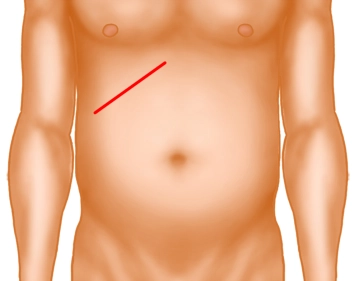
Bevorzugter Zugangsweg ist die quere Oberbauchlaparatomie rechts. Dieser Schnitt kann beliebig nach links erweitert werden. Bevor sich die laparaskopische Operation durchsetzen konnte, wurde tradionell der Rippenbogenrandschnitt rechts (nach Kocher) (s. Bild oben) empfohlen.
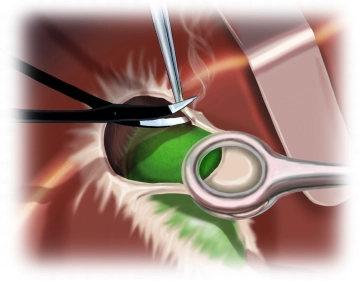
Nach Durchtrennen der Haut wird das Unterhautfettgewebe bis auf das vordere Blatt der Rektusscheide scharf durchtrennt. Dann wird die Faszie eröffnet und der Rectus abdominis mit der Diathermie quer durchtrennt. Durch Zuhilfenahme einer Kocherrinne, welche stumpf unter den Muskel geschoben wird, können thermische Verletzungen dorsaler Strukturen vermieden werden. Im lateralen Teil des Schnittes werden M. obliquus externus, internus und M. transversus abdominis durchtrennt. Die dann freiliegende hintere Rektusscheide/ Fascia transversalis wird zusammen mit dem Peritoneum vorsichtig unter Schonung intraabdomineller Strukturen eröffnet.
Anmerkung:
Pararektalschnitte sind obsolet.
Die Länge des Schnittes richtet sich immer nach den individuellen Umständen.
Niemals direkt am Rippenbogen schneiden, da in diesem Fall nicht genung Gewebe zum Wundverschluß zur Verfügung steht.
Bei vergrößerter Leber kann der Schnitt auch deutlich kaudaler erfolgen.