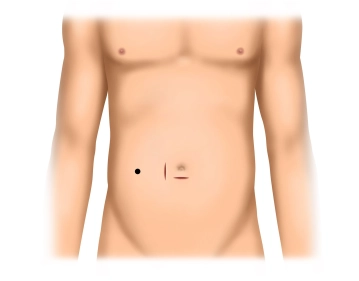
Infraumbilikale Hautinzision, Durchtrennung der Subkutis und Darstellung der Faszie.
-
Infraumbilikaler Zugang
![Infraumbilikaler Zugang]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann. -
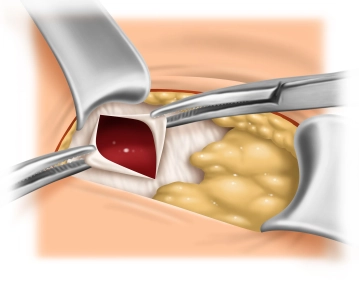
Darstellung der Nabellücke
![Darstellung der Nabellücke]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann.Bei Vorliegen einer Nabellücke (wie im Filmbeispiel) wird diese als Trokarzugang benutzt. Dazu erfolgt die stumpfe bzw. digitale Umfahrung des Nabels und Darstellung seiner Insertion auf Faszienniveau. Hier wird der Nabel scharf abpräpariert und die Nabellücke so dargestellt. Anschließend Fassen der Faszienränder mit Mikulicz-Klemmen.
Tipp:
Nabellücken müssen bei geplanter Peritonealdialyse sorgfältig versorgt werden, da es ansonsten infolge des intraabdominell instillierten Dialysats zur Hernienbildung kommen kann. Liegt keine Nabellücke vor, die als Trokarzugang genutzt werden kann, wird dieser wie bei jeder anderen Laparoskopie geschaffen. -
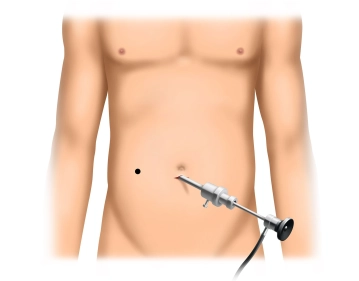
Anlegen des Pneumoperitoneums und Inspektion der Abdominalhöhle
![Anlegen des Pneumoperitoneums und Inspektion der Abdominalhöhle]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann.Einführen des Optiktrokars über eine kleine Inzision des Peritoneums und druckkontrolliertes Anlegen des Pneumoperitoneums. Einbringen der Optik und Inspektion der Abdominalhöhle, insbesondere auf evtl. Adhäsionen, die für die Seitenwahl der Katheterimplantation entscheidend sein können. Im Filmbeispiel finden sich Adhäsionen nach vorangegangener konventioneller Appendektomie, die einer rechtsseitigen Katheterimplantation allerdings nicht im Wege stehen und daher belassen werden.
-
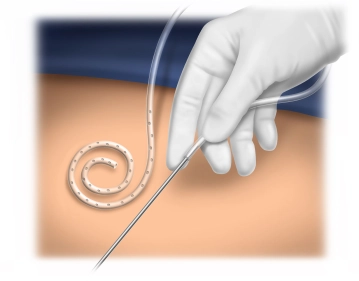
Auffädeln des Katheters
![Auffädeln des Katheters]()
Toneinstellungen Die Videosequenz kann mit einer automatischen Vertonung des darunter stehenden Textes abgespielt werden.
Sie können den automatischen Start der Vertonung als registrierter Nutzer in der Seitenleiste an- oder abstellen.
Bemerkung: Es handelt sich um eine Computerstimme, die nicht jeden Fachbegriff korrekt aussprechen kann.Der Katheter wird auf einen Führungsstab aufgefädelt. Damit bei diesem Manöver der Katheter nicht versehentlich verwrungen wird, muss die am Katheter sichtbare Strichmarkierung durchgehend in einer Linie liegen.
Tipps:
- Das Auffädeln des Katheters gestaltet sich einfacher, wenn er vorher mit NaCl-Lösung durchgespült oder darin gewässert worden ist.
- Das Coiling des Katheters sollte immer nach lateral weisen (im Filmbeispiel bei Implantation über den rechten Unterbauch also nach rechts). Weist das Coiling nach der Implantation nach medial, hat der Katheter die Tendenz, das Coiling nach lateral zu verlagern, wodurch es zu Katheter-Dislokationen aus dem kleinen Becken kommen kann.
Hautinzision zwischen Nabel und dem geplanten Katheterexit über dem Rektusmuskel rechter Unterbauch
Jetzt freischalten und direkt weiter lernen.
Einzelfreischaltung
Freischaltung dieses Lehrbeitrags für 3 Tage.
Beliebtestes Angebot
webop - Sparflex
Kombiniere flexibel unsere Lernmodule und spare bis zu 50%.
87,34 $/ jährliche Abrechnung
Allgemein- und Viszeralchirurgie
Alle Lehrbeiträge in diesem Modul freischalten.
174,70 $ / jährliche Abrechnung